Plus que la consomption, c’est la combustion dont il est question ici. C’est une réaction chimique exothermique ; elle est vive, lorsqu’elle se traduit par une flamme (combustion, donc) ; c’est une explosion1 si le front de flamme dépasse la vitesse du son.
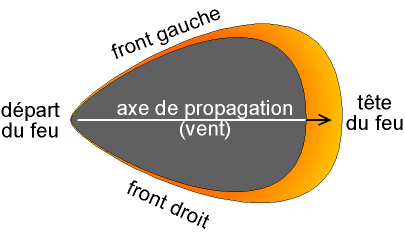
La forme du feu Lorsqu’il avance, le feu prend l’allure d’un médiator, composé d’un front de flammes et d’une traînée consumée.
Autres formes du feu Parfois le feu, selon les conditions climatiques ou thermiques peut prendre des formes particulières. Le tourbillon de feu : les différences de températures autour d’un feu de forêt ou d’un large brasier vont générer une circulation de surface des zones plus froides vers la source de chaleur. Si la masse d’air est instable, un tourbillon se formera et les débris de l’incendie y seront aspirés. Le tourbillon peut se retrouver dans la zone en flammes ou à l’extérieur, et propage l’incendie en projetant des tisons à de grandes distances. L’embrasement généralisé éclair (EGE), appelé saut de feu en québécois, est un phénomène thermique ; lorsqu’un feu se développe dans un local semi-ouvert, il se produit une alimentation convenable de l’incendie en oxygène et une accumulation de chaleur. L’explosion de fumée (EF), un afflux soudain d’air dans un local clos conduit à une explosion.
Vie et mort de l’incendie On parle, faut-il le noter, d’éclosion, de croissance jusqu’au feu constitué, puis de déclin et d’extinction. A noter que le feu se propage par rayonnement, conduction, convection, projection.
La réaction chimique se produit lorsque sont réunis quatre éléments : un combustible, un comburant, une énergie d’activation en quantités suffisantes ; il se rajoute un quatrième élément, nécessaire pour que la combustion s’entretienne et que l’on puisse parler d’incendie, la production/présence de radicaux libres.
Combustible Il y a cinq types de combustibles, qui nous donnent les cinq classes de feu :
- un solide formant des braises (bois, papier, carton, tissu, PVC, etc.) ;
- un liquide ou solide liquéfiable (essence, gazole, huile, kérosène, polyéthylène, polystyrène, etc.) ;
- un gaz (butane, propane, méthane, dihydrogène, etc.) ;
- un métal (fer, aluminium, sodium, magnésium, etc.) ;
- une huile de cuisson.
Le Comburant est l’autre réactif de la réaction chimique. La plupart du temps, il s’agit de l’air ambiant, et plus particulièrement de l’un de ses composants principaux, le dioxygène. En privant un feu d’air, on l’éteint. Dans certains cas très particuliers (souvent explosifs comme avec l’aluminium), le comburant et le combustible sont un seul et même corps; par exemple la célèbre nitroglycérine, molécule instable comportant une partie oxydante greffée sur une partie réductrice.
Activateur La réaction est déclenchée par une énergie d’activation, généralement de la chaleur ou une flamme. Par exemple, ce sera l’échauffement par frottement pour une l’allumette, le câble électrique suralimenté qui chauffe l’isolant, ou une autre flamme (propagation du feu), l’étincelle (de l’allume-gaz, de la pierre du briquet ou celle provoquée par un appareil électrique qui se met en route ou s’arrête.
Radicaux libres Dans toute combustion, des radicaux libres sont créés (par rupture de liaison chimique due à l’énergie thermique), ils vont pouvoir agir sur les autres molécules du produit (libérant d’autres radicaux libres) et engendrant de fait une réaction en chaine qui va perdurer tant que les deux conditions suivantes seront réunies : présence de combustible et de comburant.
NA. Travail à partir de Wikipédia.
- On emploie le terme déflagration lorsque le front de décomposition se déplace à une vitesse inférieure à la vitesse du son dans le milieu local, et de détonation lorsque le front de flamme dépasse la vitesse du son des gaz brûlés, ce qui engendre une onde de choc. ↩